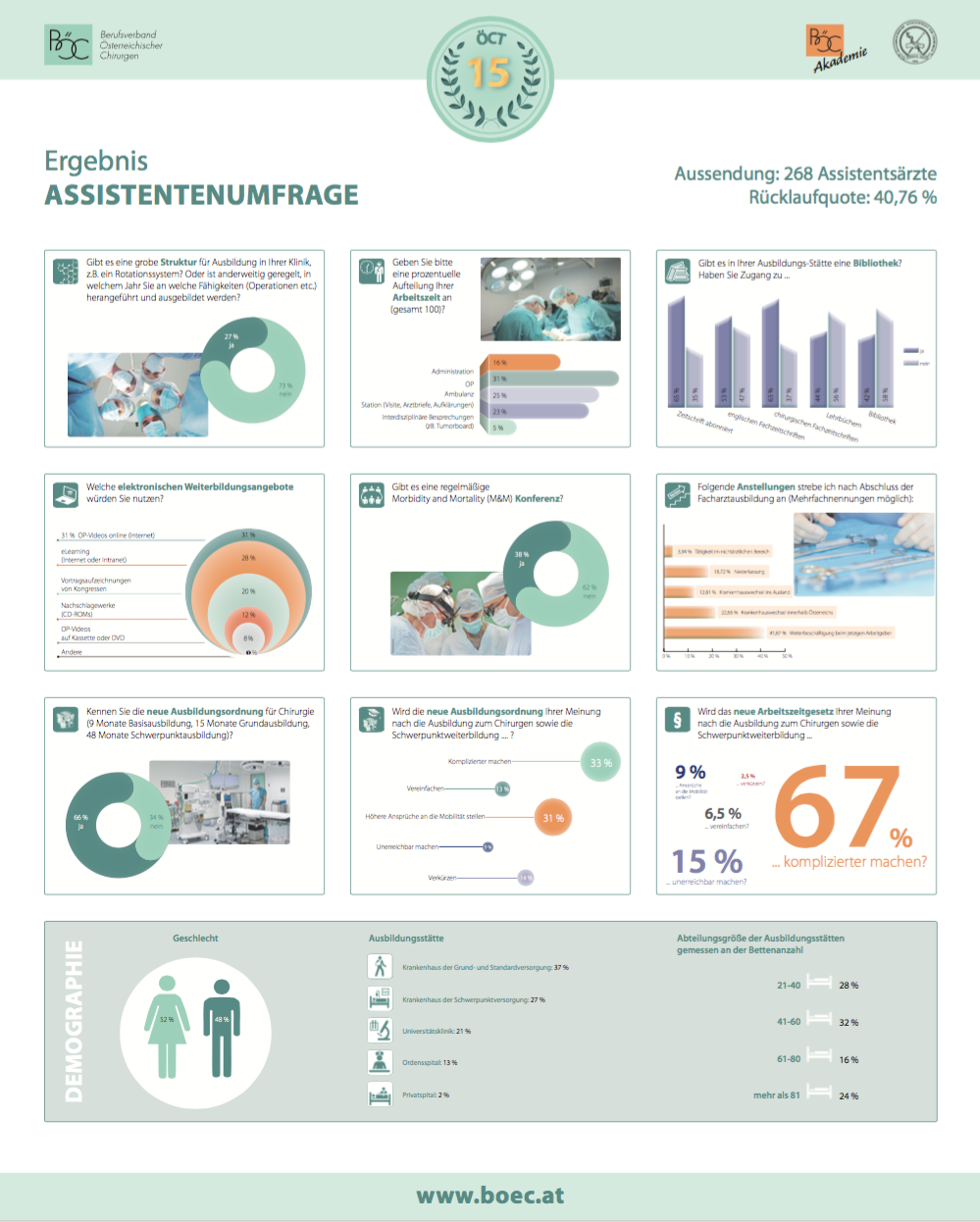
Ergebnisse der Umfrage von Fr. Dr. B. Klugsberger zur Ausbildungssituation in Österreich
Archiv für den Monat: November 2015
Nachlese 10th International Society of Laparoscopic Colorectal Surgery
Kongressbericht
10th International Society of Laparoscopic Colorectal Surgery (ISLCRS) Congress
Laparoskopische Darmchirurgie
3. bis 6. November 2015, Singapur
von Prof.Dr.Albert Tuchmann
Der 10. Internationale Kongress für laparoskopische kolorektale Chirurgie fand vom 3. bis 6. November 2015 in Singapur, Singapur General Hospital, statt.
Am ersten Kongresstag operierten die Professoren Leroy (Straßburg), Kim (Korea), Stevenson (Australien), Law (Hong Kong), Meurette (Straßburg) und Boni (Italien). Folgende Eingriffe (Live Surgery) wurden gezeigt: 3D Rektopexie, 3D Hemikolektomie rechts mit laparoskopischer mesokolischer Exzision, Robotic Surgery (Rektopexie, anteriore Resektion), vordere Resektion mit Indocyanine Perfusion. Alle Eingriffe wurden laparoskopisch durchgeführt.
Im Folgenden wird von den Kongresstagen 1 (5. November 2015) und 2 (6. November 2015) berichtet:
Delaney (USA) über Standardisierung der laparoskopischen TME:
Er weist auf Heald hin, der in seiner Erstpublikation (TME), die an 500 Patienten erzielten Ergebnisse zeigte, wenn man statt der herkömmlichen Operation die TME angewendet hat: 3 % Mortalität, 12 % Anastomoseninsuffizienz, praktisch keine Lokalrezidive. Es kommt auf den circumferentiellen Resektionsrand an! In einer schwedischen Studie, die das norwegische Konzept (entsprechend Heald) anwendete, werden die mit der TME erzielten hervorragenden Ergebnisse hinsichtlich Lokalrezidiv dargestellt (Wibe, BJS bzw. Colorectal Disease 2003).
Die TME muss daher standardisiert sein, in USA Guidelines, in England: Lapco
Weitere wichtige Publikation zu TME: Surg. Endosc. 2011;25:1136, sowie Miskovic, Ann.Surg.2014.
SAGES: Die haben ein Skills Assessment, ….. Schritt für Schritt werden gelehrt.
Auch der Simulator spielt bei der Standardisierung eine Rolle.
Ebenso haben das Royal College of Surgeons (RCS) sowie die American Society of Colorectal Surgeons (ASCRS) ihre Standards.
Konishi (Japan) über laparoskopische D3 Lymphadenektomie beim Kolonkarzinom:
20.000 Operationen wurden erfasst.
D3 Lymphadenektomie beim Kolon heißt, dass die Arteria mesenterica superior dargestellt und lymphadenektomiert wird, beim Rektumkarzinom und D3 ist es die Arteria mesenterica inferior.
Voraussetzung: Bei T1 Tumoren sind 90 % der Patienten Lymphknoten negativ, bei T3 Tumoren nur mehr 50 %.
In die Studie aufgenommen wurden T3 oder T4a Tumore. Alle M0 (Tumorgröße unter 8 cm; es dürfte keine Ileus vorliegen, oder anders gesagt: nur UICC II und III Fälle.
Neoadjuvant erhielten die Patienten 5 FU und Leucovorin bei UICC Stadium III.
Alle Fälle wurden D3 lymphadenektomiert.
Ergebnisse: 1.050 Fälle, 550 laparoskopisch, 500 offen operiert. 30 Spitäler haben teilgenommen.
Anzahl der dissezierten Lymphknoten: 20 beim offenen, 21 beim laparoskopischen Vorgehen.
5-Jahres-Überleben: 90 % beim offenen, 91 % beim laparoskopischen Verfahren.
Detailergebnis: Die offene Chirurgie ist besser beim Befall von N2 Lymphknoten und bei Patienten mit BMI > 25.
Leroy (Straßburg) zeigt alle fortgeschrittenen Verfahren, auch kombinierte und Rendezvous-Verfahren: Polypektomie, Endomukosaresektion, Endoscipic Full Thickness Resection (Literatur Brigic BJS 2013).
Weiters Endoluminal Wedge Mechanical Resection: Der Tumor (von Leroy “nodule” genannt) wird in den Hämorrhoidalstapler „hineingedrängt“ und dann durch Schließen des Hämorrhoidalstaplers mit einer schmalen Rektummanschette reseziert.
Dann gibt es noch die Full Notes Transanal Sequential Colonic Resection (Transanale Sigmaresektion). Ein Video wird gezeigt. Ähnliches Vorgehen ist nachzulesen bei Lamm, Andreas Zerz u.a. JACS 2015;221, 789-797).
Auch eine Cörcum-Polresektion wird gezeigt mit kombinierter Koloskopie und Laparoskopie unter Zuhilfenahme eines sogenannten „Lift“, das ist ein T-förmiges Plastikstück, das in das Cöcum eingestochen wird um das Cöcum anzuheben und den Cöcum-Pol abhebeln zu können.
Wong (Singapur) über ventrale Rektopexie für Rektumprolaps:
Er weist zuerst auf die verschiedenen Symptome und Begleiterkrankungen, z.B. Rektozele, hin und erwähnt die alternativ zur Anwendung kommenden Verfahren:
- posteriore Rektopexie mit mehr als 50 % Obstipation als postoperative Folge
- Delorme, ein transanales Verfahren mit hoher Rezidivrate und hoher Rate an Stuhlinkontinenz
- Mesh-Verfahren gibt es seit Wells (1958)
- Wexner: Resektion und Rektopexie
- Ventale Rektopexie mit Mesh, die auf D’Hoore zurückgeht
Literatur bei Wong, doi 10.1111 Online-Publikation, Roboter assistiert
doi 10.1111/codi 12164, das ist eine Metaanalyse hauptsächlich hinsichtlich Komplikationen.
Es gibt ein Konsensus-Paper von Mercer Jones und D’Hoore: Colorec.Dis. 2013;16:82-89).
In einem Lunch-Symposium (Olympus) wurden die Eigenschaften von Thunderbeat und 3D Laparoskopie demonstriert.
Stevenson (Australien) berichtete über TAMIS (Transanal Minimal Invasive Surgery):
SIL hätte keinen Fortschritt gebracht, die üblichen Multicenterstudien, Color II, Classic sowie die koreanische Studie und andere werden zitiert.
Die Erstpublikationen über TAMIS sind von M. Albert sowie von Sylla und Lacy.
Es gibt noch die Termini TaTME (Transanale TME) sowie TATA ROBOT. Insgesamt kommt es in erster Linie auf eine gute Tabaksbeutelnaht an!
In Australien gibt es ein Register von 500 Fällen, siehe auch www.ausces.com.
John Marks (USA) berichtete über den Stand der Studien hinsichtlich TAMIS (bzw. TaTME):
Einige Studien werden zitiert, z.B. ACOSOOG Z6051, die Zahl der Publikationen hat zugenommen: Laut PubMed in den Jahren 2009 und 2010 je eine Studie, 2013 14 Studien, 2014 19 Studien über dieses Thema.
Zusammenfassend ist TAMIS vorteilhaft bei engem Becken, Adipositas und größerem Tumor (Bulky Tumor).
Die operierten Tumore waren duchwegs unter 6 cm und wurden mit 4500 bis 6000 Gy vorbestrahlt.
Operationstechnik (Video) mit der Diathermie wird inzidiert, dann mit der Schere zwischen Rektum und Puborektalis präpariert, dann erfolgt die Tabaksbeutelnaht.
Conclusion: Die Technik (TAMIS, TaTME, TATA) ist machbar, sowohl technisch als auch makroskopisch-pathologisch (komplette TME!). Für die Zukunft wichtig ist die Festlegung einer standardisierten Technik, randomisierte Studien sowie langzeitonkologische Ergebnisse.
Kam (Singapur) über minimal invasive Hämorrhoidektomie:
Gezeigt wird das Longo-Verfahren. Probleme des Verfahrens, zitiert aus der Literatur, seien persistierender Prolaps (10 %), dringliche Stuhlentleerung (bis zu 40 % !!!?) sowie inkomplette Entleerung. Der Referent selbst berichtet über 7000 Fälle (Longo).
Postoperative Komplikationen: Urinretention 4 %, postoperative Blutung (OP-bedürftig) 0,3 % mit insgesamt 36 Blutkonserven (bei 7000 Fällen), 1,7 % Schmerzen, 1,2 % Strikturen.
Anastomoseninsuffizienz 7 von 7000 (0,1 %).
Rezidiv 14 = 0,2 %
Laut Nachuntersuchung mit Fragebogen (n = 1835): Besserung des Leidens 95 %; 1 % Stuhlinkontinenz, dabei achte man auf glatte Muskelzellen im histologischen Präparat !!!
Tan (Singapur) über Analfisteln:
Innovative Verfahren wie verschiedene ……. verfahren sowie die Fistuloskopie und Reinigung des Fistelkanals mit einer „Bürste“ werden gezeigt.
Es folgt eine Videositzung:
Delaney (USA) hat ein Buch geschrieben mit genauer Darstellung der laparoskopischen Technik, Nettr Surgical Process 2013. Er verwendet die Schere mit elektrischem Strom um genau in der Schicht zu präparieren. Zum „Weghalten“ verwendet er einen Fan Retractor (fächerförmig), damit verhindert er das Einreißen des Mesos (er verwendet deswegen keinen „Grasper“). Das Einreißen des Meso passiert hauptsächlich bei Adipösen.
Eine Studie im NEJM von Donjer und Mitarbeitern wird zitiert; verglichen wurde Rektum offen versus laparoskopisch. Im mittleren Drittel war das offene Verfahren besser, im unteren Drittel das laparoskopische; Lokalrezidiv 11 % bei offener Technik, 4 % (!!) bei laparoskopischer.
Der Linear Stapler zum Abstapeln des Rektums wird vom Port im rechten Oberbauch eingeführt, das ist die Stelle, an der später das Ileostoma angelegt wird.
Delaney betont, dass zum Abstapeln des Rektums ein Staplermagazin, maximal zwei ausreichen sollen. Damit werden die lateralen Zipfel, „Ohren“, der Staplernaht verhindert, die bei Double Stapling Technik möglicherweise später zur Anastomoseninsuffizienz führen.
Transanale TME sollte nur bei Männern, bei BMI von etwa 40 und dem unteren Rektumdrittel durchgeführt werden; möglichst mit Häkchen und Diathermie – Delaney ist gegenüber der transanalen TME eher reserviert! Seine Patienten haben eine Lokalrezidivrate von 3 %.
Kim (Korea) berichtet über D3 Lymphadenektomie bei der Hemikolektomie rechts und bei der Hemikolektomie links (Video):
Er beschreibt eine 6-Stufen-Technik, die eine No-Touch-Isolation-Technik beinhaltet. Wichtig dabei ist die hohe Ligatur sämtlicher Gefäße (Ileokolika, Kolika media, usw.). Es wird ausschließlich mit Häkchen und „Backhand“ präpariert.
Dabei verwendet er ein Instrument, das wie ein Sauger aussieht (auch stumpfe Präparation möglich), in dem aber ein Häkchen, das vorgeschoben werden kann, integriert ist !!
Auffallend ist die Schlankheit des Patienten, wobei man den linken Ureter durch das Peritoneum durchsieht.
Law (Hong Kong), ebendort Chairman und Präsident der International Society of Laparoscopic Colorectal Surgery, berichtet von zu erwartenden Anastomoseninsuffizienzen bei ileokolischer Anastomose 2,5 bis 7 %, bei Kolon-Kolon-Anastomose 3 bis 6 %, kolorektaler Anastomose 3 bis 8 % und Rektumanastomose über 10 %. Bei der Hemikolektomie rechts macht er zwei Haltenähte, dann eine kleine Enterotomie sowie eine kleine Kolotomie zur Einführung des Linear Staplers, dann wir gestapelt, zuletzt fortlaufende Naht der Enterotomie.
Fluoreszenzangiographie: Indocyanin-Injektion zeigt gute Durchblutung sowohl des Kolons als auch des Rektumstumpfes, Literatur bei Jafari, JACS 2015.
Leakage Test: Luftinsufflation unter Wasser sowie intraoperative Koloskopie; Literatur bei Li VK (aus der Wexner-Gruppe) Surg.Endosc. 2009: routinemäßige Koloskopie !
Besonderes technisches Vorgehen: Präparatbergung durch Rektum; dazu Rektotomie, Einlage einer Wundrandschutzfolie und transanale Präparatbergung; danach Tabaksbeutelnaht am Rektumstumpf, dann Durchführung der Anastomose; Vorteil: durch Vermeidung des Double Stapling keine „Dog Ears“; dieses Operationsverfahren ist allerdings nur durch Roboterchirurgie möglich, sonst (Tabaksbeutelnaht) zu schwierig.
Boni (Varese, Italien) zeigt die transvaginale Präparatbergung, er verwendet den Terminus NOSE; n = 196 Studienfälle; transvaginale gegen transumbilikale (Minilaparotomie) Präparatbergung. Ergebnisse: Hauptvorteil beim transvaginalen Vorgehen ist der geringere Schmerz. Die Kolpotomie muss aber immer als posteriore Kolpotomie erfolgen, dann gäbe es keine Dyspareunie.
OP-Technik: Die Kolpotomie wird mit dem Diathermiehäkchen vom Bauch her durchgeführt, wobei der transvaginal eingeführte Endobag gegen das Diathermiehäkchen gedrängt wird. Die Kolpotomie (posterior !) wird betont klein gehalten, da die Vagina dehnbar ist. Eine Wundrandschutzfolie wird verwendet, ebenso eine Fluoreszenzangiographie.
Beim Mann kann die Präparatbergung transanal erfolgen, jedoch nur bei gutartigen Prozessen; am Rektum wird dann eine Tabaksbeutelnaht angelegt. Vorher wird die Andruckplatte des Circular Staplers durch den Rektumstumpf eingebracht.
Roxas (Philippinen) spricht über kolorektales Karzinom Stadium IV. Aus den Philippinen sind 20 bis 30 % der Patienten im Stadium IV, 30 bis 40 % im Stadium III; 30 % haben bereits eine Karzinosis peritonei, das 5-Jahres-Überleben beträgt beim Kolonkarzinom insgesamt 40 bis 50 %. Alle stenosierenden Rektumkarzinome bekommen vorerst ein Stoma.
Wegen der hohen Prävalenz der Karzinose gibt es relativ viel HIPEC-Patienten, etwa 30 Patienten in zwei Jahren.
Literatur Basingstoke, Moran und Cecil online doi 10.1002/bjs
Melissa Teo, Int.J.Cr.Dis. 2014;29:895-898
Pionier der HIPEC ist Sugarbaker: Surgery 1985;98:414
Nach Elias Europ.J.Surg. sowie Verwaal ist ein 5-Jahres-Überleben von 20 bis 50 % möglich. Mit der besten Chemotherapie ist ein Überleben bis zu 24 Monaten möglich. Die Ergebnisse mit HIPEC hinsichtlich medianer Überlebenszeit sind doppelt so gut wie mit der besten systemischen Chemotherapie, weil die Karzinose häufig eine rein lokale Erkrankung ist. Die Konzentration des Chemotherapeutikums am Peritoneum ist bei HIPEC 1000-fach so hoch wie bei systemischer Chemotherapie. Bei der HIPEC werden eine Peritonektomie gemacht, eine lokale Chemotherapie sowie eine Hyperthermie. Zur Beurteilung der objektiven Ergebnisse ist ein Scoring der Karzinose notwendig.
Melissa Teo (Singapur) über zytoreduktive Chirurgie und HIPEC:
WJS 2006;30:2132-2135:
201 Fälle, OP-Zeit 6 bis 7 Stunden, 5-Jahres-Überleben 40 % !!!; 36 % postoperative Komplikationen, davon die Hälfte schwer, jedoch nur 0,5 % Mortalität.
David Jayne (England) über Lernkurve bei laparoskopischer sowie Robotic Colorectal Surgery:
Insgesamt werden 5 bis 300 Fälle Lernkurve angegeben; andererseits n = 55 für Rechtsresektion, n = 62 für Linksresektion, wobei folgende Messparameter herangezogen werden: OP-Zeit, Umstieg, Blutverlust, postoperativer Aufenthalt in Tagen, Morbidität, Mortalität, Lymphknotenentnahme (Anzahl).
Literatur Kayano Surg.Endosc. 2011
Jennifer Bari: Ann.Surg.Oncol. 2014
Jedoch nur 20 (15 – 30) Fälle für Robotic.
Marks (USA): bevorzugt koloanale Anastomose, Rektumkarzinom möglichst mit Schere und wenig Strom präparieren, Präparatbergung transanal 1000 Fälle; 5 mm im Gesunden reseziert genügt; unter neoadjuvanter Chemotherapie 90 % 5-Jahres-Überleben !!
Laut David Jayne (England) gibt es seit Einführen eines nationalen Programms in Großbritannien 50 % … A Fälle !!
Stevenson (Australien) über Pelvic Floor Surgery (Rektumprolaps, Inkontinenz):
- ventrale Rektopexie
- Sphinkterrepair (80 % Erfolge)
- Gracilis-Plastik
- Phenix (wie der Magnetring bei Fundoplikatio)
- TOPAS-Sling (das ist ein Band aus Prolene)
- SNS (sakrale Nervenstimulation, Neuromodulation)
Literatur Altomare BJS; ventrale Rektopexie bei D’Hoore Surg.Endosc. 2006; 20:1919-1923
Meshes können zu Erosionen führen; persönliche Zahlen von Stevenson 231 Fälle zwischen 2008 und 2014; biologisches Mesh ist besser als Prolene hinsichtlich Rezidiv; eine komplette Remission der Stuhlinkontinenz ist in 50 % möglich; siehe auch www.ausces.com
Mittagssymposium:
Leroy (Straßburg) zeigt ein Video einer tiefen vorderen Resektion; dabei verwendet er zum Weghalten z.B. der Harnblase einen speziellen Retraktor, das ist ein 10 mm-Stiel mit einem kleinen (etwa 2 cm) abwinkelbaren Stück an der Spitze, welches L-förmig, H-förmig oder V-förmig abgewinkelt werden kann (Fa. Storz). Die Abwinkelung erfolgt mit einer Stellschraube von außen. Dadurch ist eine hervorragende Exposition des Operationsgebietes, z.B. bei der TME, möglich. Leroy nimmt dabei nur das Häkchen zum Präparieren, das Rektum setzt er mit zwei 30 mm-Magazinen ab. Vorher ligiert er das Rektum proximal der geplanten Absetzungsstelle um damit besser nach kranial ziehen zu können.
Boni (Italien) zeigt Fluorescent Lymph Node Mapping; n = 15; zeigt Metastasierungsweg mit Anfärbungen an Arteria ileocolica (Stamm) oder colica media; funktioniert ähnlich dem Sentinel Lymphknoten, der Farbstoff wird peritumoral injiziert; ICG Fluoreszenz.
Podiumsdiskussion über Roboterchirurgie:
Franklin und Leroy halten sie eher für überflüssig, Asiaten (Lee, Choi, Law, Kuo) sind dafür. Es gibt eine Rollar-Studie, die der Roboterchirurgie keinen eindeutigen Vorteil ausweist.
Nachlese ACO-ASSO JT (Schilddrüsenkarzinom)
Erweiterte und multiviszerale Eingriffe beim fortgeschrittenen Schilddrüsenkarzinom
von Rudolf Roka
Die Herausforderung bei der Chirurgie organüberschreitender Schilddrüsenkarzinome (OSC) liegt im adäquaten Resektionsausmaß um sowohl der Radikalität als auch dem Funktionserhalt gerecht zu werden. OSC weisen einen eklatant höheren Prozentsatz an histologisch aggressiven Formen auf. Die Häufigkeit liegt zwischen 4% und 7% scheint jedoch in letzter Zeit durch die hohe Rate präventiver Eingriffe zurückzugehen.
Therapeutisch anspruchsvoll ist die Infiltration in Trachea, Larynx, Hypopharynx, Ösophagus und die großen Gefäße. Die häufigste Form des OSC in den Larynx ist das An- oder Umwachsen des Nervus laryngeus recurrens, zumeist nahe seiner Einmündung in die Larynxmuskulatur.
- Bei intaktem Nerven sollte ein “Shaving” durchgeführt werden, wenn eine makroskopisch vollständige Tumorentfernung möglich ist. Eine anschließende Radio-Jod-Therapie bei differenziertem OSC ist obligat.
- Ist der Nerv bereits funktionslos ist eine Neurolyse nicht erfolgreich und der Nerv sollte reseziert werden. Die Infiltration der Trachealwand, vor allem jedoch die intramurale Tumorausbereitung ist nicht abschätzbar. Das bedeutet, dass ein „Shaving“ nur bei ganz oberflächlicher Adhärenz des Tumors zur Anwendung kommen sollte. Onkologisch am verlässlichsten ist somit die Vollwandresektion, vor allem als Querresektion. Aufgrund des Operationsrisikos ist ein derartiger Eingriff in Zusammenschau mit folgenden Faktoren abzuwägen: Allgemeinzustand, Alter und Lebenserwartung des Patienten, Histologie, Grading und Tumorstadium. Bei differenziertem OSC beträgt die Latenzzeit zwischen (inkomplettem) Shaving und therapiepflichtigem Lokalrezidiv im Mittel 67 Monate.
Nahtverschlüsse an Hypopharynx und Ösophagus sind aufgrund mangelnder Mobilisierungsmöglichkeiten Dehiszenz-gefährdet. Größere transmurale Defekte erfordern die Rekonstruktion mit frei transplantiertem Jejunum. Während die großen Venen relativ häufig von Tumor infiltriert sein können und entweder reseziert (Vena jugularis interna) oder rekonstruiert (Vena subclavia, Vena cava) werden, sind Arterien nur ausnahmsweise betroffen bzw. die Resektion/Rekonstruktion selten indiziert. Als Zugang zum Mediastinum eignet sich bei Prozessen im Mittelfeld die partielle oder totale Sternotomie, bei Prozessen im lateralen Mediastinum die partielle Sternotomie mit Verlängerung in den Interkostalraum der betroffenen Seite.